Buona capitalizzazione fino al 2026 con
capacità di finanziamento al 100% dell'asset principale EryDex, con
in programma uno studio di fase 3 sottoposto a valutazione speciale
del protocollo (SPA, Special Protocol Assessment) e la
presentazione di una richiesta di approvazione di nuovo farmaco
(NDA)
EryDex utilizza la tecnologia di incapsulamento
intracellulare autologo di farmaci (AIDE) progettata per il lento
rilascio di steroidi nell'arco di diverse settimane senza la
tossicità a lungo termine tipicamente associata alla
somministrazione cronica
Vi è il potenziale per una rapida espansione di
EryDex verso altre indicazioni per malattie rare e debilitanti, in
cui il trattamento cronico con steroidi rappresenta, o può
diventare, lo standard di cura
Quince Therapeutics, Inc. (Nasdaq: QNCX), azienda biotecnologica
focalizzata sull'acquisizione, lo sviluppo e la commercializzazione
di terapie innovative che trasformano la vita dei pazienti, oggi
annuncia di aver sottoscritto un accordo per l'acquisizione di
EryDel SpA, azienda privata di biotecnologie in fase avanzata, nel
quadro di uno scambio azionario anticipato e con potenziali futuri
pagamenti in contanti legati ai risultati. EryDel ha sviluppato
AIDE, una tecnologia di incapsulamento intracellulare autologo di
farmaci, ed EryDex, un asset principale di fase 3 mirato a una rara
malattia neurologica pediatrica mortale, l'atassia-telangectasia
(A-T), che attualmente non dispone di trattamenti approvati. Una
volta perfezionata la transazione, gli azionisti di EryDel
deterranno circa il 16,7% della società combinata (soggetta a una
rettifica al ribasso) e avranno diritto a un massimo di 485 milioni
di dollari USA in caso di pagamenti legati a obiettivi di sviluppo,
normativi e commerciali, a esclusione delle royalty. Approvata
all'unanimità dai consigli di amministrazione di entrambe le
aziende, la transazione è soggetta a determinate approvazioni di
legge e ad altre condizioni di perfezionamento, e dovrebbe
concludersi nel terzo trimestre del 2023.
Il Dr. Dirk Thye, Chief Executive Officer di Quince, ha
commentato: "Siamo estremamente entusiasti e ottimisti riguardo
all'acquisizione di questa esclusiva piattaforma
farmacologica-tecnologica combinata, nonché del promettente asset
clinico in fase avanzata, che promuoverà la prossima fase della
crescita di Quince. La tecnologia AIDE brevettata di EryDel
consente l'incapsulamento intracellulare autologo e la
somministrazione di desametasone con rilascio lento e controllato,
con il potenziale per consentire la somministrazione cronica di
steroidi per mesi o anni con un profilo di sicurezza favorevole.
Questo rappresenta non solo un'enorme opportunità mirata all'A-T,
ma offre anche il potenziale per espandersi verso diverse malattie
rare debilitanti in cui il trattamento cronico con steroidi è lo
standard di cura, o potrebbe esserlo in assenza di tossicità
steroidea a lungo termine. Al termine dell'acquisizione, in caso di
risultati positivi concentreremo rapidamente la solida competenza
nello sviluppo che ci contraddistingue e le risorse finanziarie per
promuovere l'asset principale EryDex per l'A-T tramite un unico
studio clinico globale di fase 3 tramite una SPA e una NDA
anticipata già depositate presso la FDA".
Luca Benatti, Chief Executive Officer di EryDel, ha commentato:
"L'acquisizione di EryDel da parte di Quince offre l'opportunità di
promuovere la nostra innovativa tecnologia di incapsulamento
intracellulare autologo presso i punti di cura, dallo sviluppo alla
commercializzazione, e di realizzare la nostra missione: fornire il
primo trattamento per i pazienti colpiti da A-T, una malattia
devastante. L'impegno di Quince sarà supportato dagli incoraggianti
dati di fase 3 generati dal precedente studio internazionale di
EryDel su EryDex, che hanno dimostrato un significativo ritardo
nella progressione della malattia nei pazienti A-T, a ulteriore
supporto di oltre 10 anni di dati sulla sicurezza. Quince è ben
posizionata per far progredire la tecnologia differenziata AIDE di
EryDel e per lo sviluppo di EryDex, il nostro asset principale, per
fornire trattamenti innovativi ai pazienti che ne necessitano".
Un'acquisizione trasformativa con pietre miliari cliniche che
generano valore
I punti principali dell'acquisizione di EryDel includono:
Buona capitalizzazione fino al 2026, con la capacità di
finanziare al 100% l'asset principale EryDex e previsioni di
iniziare lo studio clinico di fase 3 con richieste SPA e NDA
- Solidità del bilancio, con circa 87,6 milioni di dollari USA in
contanti, equivalenti in contanti e investimenti a breve termine
(non sottoposti ad auditing) al 30 giugno 2023, per fornire
finanziamenti mirati alle esigenze operative fino al 2026.
- Un efficiente programma di sviluppo dal punto di vista del
capitale consente il finanziamento di EryDex per tutto lo studio
clinico globale di fase 3 con la richiesta SPA e, in caso di
risultati positivi dello studio, con la richiesta NDA, oltre a
effettuare attività nel quadro delle normative europee relative
alla potenziale presentazione MAA.
- Possibilità potenziali di concessioni in licenza per territori
regionali al di fuori degli Stati Uniti, per facilitare
l'approvazione normativa di EryDex.
Piani di arruolamento del primo paziente in uno studio globale
di fase 3 su EryDex nel secondo trimestre del 2024, con la
richiesta NDA prevista entro la fine del 2025
- SPA in corso presso la FDA per un unico studio clinico globale
di fase 3 su EryDex che, secondo le previsioni, dovrebbe essere
sufficiente per la richiesta NDA, in caso di risultati positivi
dello studio.
- EryDex designato come farmaco orfano per il trattamento
dell'A-T, sia da parte della FDA che dell'EMA.
- Lo studio clinico di fase 3 NEAT (Neurologic Effects of
EryDex on Subjects with A-T) è uno studio programmato
di efficacia globale in doppio cieco, randomizzato e controllato
con placebo, su circa 86 pazienti A-T dai sei ai nove anni, con
ulteriori altri 20 pazienti di almeno 10 anni inclusi per un
potenziale supporto più ampio.
- Come concordato con la FDA, l'endpoint primario è la
misurazione della funzione neurologica sulla base
dell'International Cooperative Ataxia Rating Scale modificato e
ricalcolato (RmICARS), dalla baseline al sesto mese di
trattamento.
- Gli endpoint secondari hanno misurato i punteggi Clinical
Global Impression per gravità (CGI-S) e cambiamento (CGI-C), nonché
il punteggio EuroQol per la qualità della vita.
- Previsioni di arruolamento del primo paziente nello studio
clinico di fase 3 NEAT nel secondo trimestre del 2024.
- Versione commerciale dei materiali di consumo per il
trattamento EryKit approvata in Europa e attualmente in fase di
parziale sospensione clinica, in attesa della risposta a una
domanda della FDA.
- L'obiettivo è la presentazione della richiesta NDA per EryDex
presso la FDA entro la fine del 2025, in caso di risultati positivi
dello studio di fase 3 NEAT.
Profilo di efficacia e sicurezza di EryDex dimostrato in un
precedente studio clinico di fase 3 su pazienti A-T
- Effettuazione delle attività normative europee relative alla
potenziale richiesta MAA su EryDex in base a un precedente studio
clinico di fase 3.
- Completamento del maggior studio globale di efficacia su
pazienti A-T (N=175) nello studio clinico di fase 3 ATTeST
(Ataxia Telangiectasia Trial with the
EryDex SysTem) e in un'estensione a lungo
termine (OLE) (N=104).
- L'endpoint primario ha misurato il punteggio International
Cooperative Ataxia Rating Scale (mICARS) modificato, dalla baseline
al sesto mese di trattamento.
- Gli endpoint secondari hanno misurato i punteggi CGI-C, Quality
of Life (QOL) e Vineland Adaptive Behavior Scales (VABS).
- Il braccio di trattamento con dosi elevate di EryDex ha
dimostrato un rallentamento nel deterioramento neurologico nel
corso della progressione dell'A-T misurato in base al punteggio
mICARS nella popolazione con intenzione di trattamento (ITT, Intent
To Treat), con un effetto statisticamente significativo nel
sottogruppo tra i sei e i nove anni su molteplici endpoint.
- L'analisi di sicurezza a 12 mesi ha dimostrato che EryDex è ben
tollerato, senza eventi avversi importanti tipicamente associati
alla somministrazione cronica di steroidi.
- Effetto terapeutico prolungato e profilo di sicurezza
favorevole mantenuti per più di tre anni aggiuntivi nel braccio
nello studio OLE sottoposto a trattamento con alte dosi, oltre
all'assenza di tossicità steroidea correlata osservata nei pazienti
che hanno ricevuto il trattamento per oltre 10 anni.
- Marchio Conformité Européene (CE) già ottenuto in Europa per la
combinazione farmaco/dispositivo e per la versione commerciale dei
prodotti di consumo per il trattamento EryKit.
Opportunità di un picco di vendite globali stimato a oltre 1
miliardo di dollari per la sola indicazione A-T, con un potenziale
di rapida espansione di EryDex per altre malattie rare e
debilitanti
- La popolazione A-T è stimata in circa 10.000 pazienti negli
Stati Uniti, nel Regno Unito e nei paesi dell'UE4 che attualmente
non dispongono di terapie approvate, con opportunità di un picco di
vendite stimato in oltre 1 miliardo di dollari a livello
globale.
- EryDex per l'indicazione A-T ha il potenziale per essere il
primo sul mercato con prezzi comparabili interessanti e senza che
sia nota alcuna concorrenza in fase avanzata.
- EryDex è stato designato come farmaco orfano per il trattamento
dell'A-T dalla FDA e dall'EMA.
- Potenziale per la rapida espansione di EryDex verso altre
indicazioni di malattie rare e debilitanti in cui la
somministrazione cronica di steroidi rappresenta lo standard di
cura, o potrebbe diventarlo, in assenza di tossicità da steroidi a
lungo termine.
- Possibilità di espansione della piattaforma AIDE verso altri
farmaci o biologici, tra cui la terapia enzimatica
sostitutiva.
- Le tutele tecnologiche multi-sfaccettate creano forti barriere
all'ingresso, con l'esclusività sulla proprietà intellettuale fino
ad almeno il 2034 nel mondo e ad almeno il 2035 negli Stati
Uniti.
Informazioni sulla transazione
In base ai termini della transazione per l'acquisizione, EryDel
opererà come controllata al 100% da Quince Therapeutics, con
programmi mirati alla conservazione della presenza produttiva e
aziendale di EryDel in Italia. La società integrata sarà diretta
dal Dr. Dirk Thye, Chief Executive Officer di Quince e
amministratore del CdA dell'azienda. David Lamond si conferma a
presidente del CdA di Quince, che sarà composto da un ulteriore
amministratore nella persona di Luca Benatti, rappresentante di
EryDel, dopo il perfezionamento della transazione.
Al completamento dello scambio azionario anticipato, gli
azionisti di EryDel disporranno di un massimo di circa il 16,7%,
pari a 7.250.352 azioni, della società combinata (soggetta a una
rettifica al ribasso). L'accordo di transazione include fino a 485
milioni di dollari in potenziali successivi pagamenti in contanti
totali, di cui fino a 5 milioni di dollari al raggiungimento di
obiettivi di sviluppo, 25 milioni di dollari all'accettazione della
richiesta NDA, 60 milioni di dollari legati a importanti risultati
nelle approvazioni e 395 milioni di dollari al raggiungimento di
obiettivi di mercato e di vendita, senza versamento di royalty agli
azionisti di EryDel. La transazione includerà la sottoscrizione di
un prestito da 13 milioni di dollari (10 milioni di euro in
capitale) da parte di EryDel presso la Banca europea per gli
investimenti (BEI), con pagamenti programmati a partire dal secondo
semestre del 2026.
Approvata all'unanimità dai consigli di amministrazione di
entrambe le aziende, la transazione è soggetta a determinate
approvazioni di legge e ad altre condizioni di perfezionamento, e
dovrebbe concludersi nel terzo trimestre del 2023.
Rendiconto finanziario
Quince non ha completato la preparazione del rendiconto
finanziario dell'azienda per il secondo trimestre del 2023. Le
liquidità, l'equivalente liquido e gli investimenti a breve termine
presentati al 30 giugno 2023 sono preliminari e non ancora
sottoposti ad auditing e, quindi, sono intrinsecamente incerti e
soggetti a modifiche. L'azienda è impegnata nel completamento delle
consuete procedure di chiusura e revisione per il secondo trimestre
del 2023 e non vi è alcuna garanzia sulla corrispondenza dei
risultati finali relativi a questo periodo con tali importi
preliminari non sottoposti ad auditing. La società di revisione
contabile pubblica indipendente dell'azienda non ha sottoposto ad
auditing, rivisto, compilato o eseguito alcuna procedura in
relazione a tali dati preliminari per il secondo trimestre
terminato il 30 giugno 2023.
Consulenti
MTS Health Partners, L.P. svolge l'incarico di consulente
finanziario e Cooley LLP svolge l'incarico di consulente legale di
Quince. Perella Weinberg Partners svolge l'incarico di consulente
finanziario e Goodwin Procter LLP e Clifford Chance LLP svolgono
l'incarico di consulenti legali di EryDel.
Disponibilità della presentazione per gli investitori
Per ulteriori informazioni sulla transazione, gli investitori
sono invitati ad accedere a una presentazione per gli investitori
che riporta dettagli sull'acquisizione di EryDel fornita dalla
dirigenza di Quince, attualmente disponibile per la consultazione
sul sito web dell'azienda dedicato ai rapporti con gli investitori.
Per accedere alla presentazione visitare la pagina Events (Eventi),
all'intestazione News & Events (Notizie ed eventi) del sito web
di Quince dedicato ai rapporti con gli investitori, all'indirizzo
ir.quincetx.com.
Informazioni su Quince Therapeutics
Quince Therapeutics è un'azienda biotecnologica specializzata
nell'acquisizione, nello sviluppo e nella commercializzazione di
terapie innovative che trasformano la vita dei pazienti affetti da
malattie debilitanti e rare. Per ulteriori informazioni visitare il
sito www.quincetx.com, seguire Quince Therapeutics su LinkedIn e
@Quince_Tx su Twitter.
Informazioni su EryDel SpA
EryDel SpA è un'azienda biotech globale in fase avanzata
impegnata nello sviluppo e nella commercializzazione di terapie per
il trattamento di malattie rare tramite la tecnologia brevettata
dell'azienda, basata sui globuli rossi. EryDex, il suo prodotto più
avanzato, è nella fase avanzata dello sviluppo per il trattamento
dell'atassia teleangectasia (A-T), una rara malattia neurologica
autosomica recessiva per cui attualmente non è disponibile alcuna
terapia consolidata. EryDex è una tecnologia ambulatoriale
automatizzata per pazienti esterni che consente di incapsulare ex
vivo il desametasone sodio fosfato (DSP; un profarmaco) nei globuli
rossi del paziente, che vengono poi reinfusi, consentendo la
circolazione di basse dosi controllate, con il lento rilascio di
desametasone (principio attivo) nelle successive settimane
successive al trattamento. EryDex ha ottenuto la designazione di
farmaco orfano per il trattamento dell'A-T sia dalla U.S. Food and
Drug Administration (FDA) che dall'Agenzia europea per i medicinali
(EMA). Sono stati completati con successo ATTeST, uno studio
clinico multicentrico internazionale di fase 3, e la relativa
estensione a lungo termine. Oltre a EryDex, la piattaforma
tecnologica di EryDel è in grado di espandersi verso altri farmaci
o biologici, inclusa la terapia enzimatica sostitutiva, e presenta
il potenziale per supportare un'ampia gamma di opportunità
terapeutiche.
Dichiarazioni a carattere previsionale
Le dichiarazioni in questo comunicato stampa contengono
"dichiarazioni a carattere previsionale" ai sensi del Private
Securities Litigation Reform Act del 1995 come riportato nella
Sezione 27A del Securities Act del 1933, e successive modifiche, e
nella Sezione 21E del Securities Exchange Act del 1934, e
successive modifiche, soggette al "safe harbor" (porto sicuro)
creato da tali sezioni. Tutte le dichiarazioni che non
costituiscano fatti storici possono essere dichiarazioni a
carattere previsionale. Le dichiarazioni a carattere previsionale
contenute in questo comunicato stampa sono identificabili dall'uso
di termini quali "credere", "potere", "dovrebbe", "aspettarsi",
"anticipare", "programmare", "credere", "stimare", "potenziale",
"intendere", "sarà", "può", "cercare" o altri termini simili.
Esempi di dichiarazioni a carattere previsionale includono, tra
l'altro, le dichiarazioni sull'acquisizione di EryDel da parte di
Quince; la tempistica della chiusura della transazione; i benefici
previsti dalla transazione, incluso lo sviluppo clinico continuo,
attuale e futuro, e la potenziale espansione delle attività di
EryDel e della relativa piattaforma e i costi e la tempistica
relativi; il percorso di sviluppo strategico per EryDex; le
previste richieste alla FDA e all'EMA e studi clinici e
tempistiche, prospettive e aspettative fondamentali; la tempistica
e il successo deli studi clinici e i relativi dati, compresi i
piani e la capacità di iniziare, finanziare, condurre e/o
completare gli studi in corso e quelli aggiuntivi; i potenziali
benefici terapeutici, la sicurezza e l'efficacia di EryDex; le
dichiarazioni sulla capacità dell'azienda di ottenere, e la
relativa tempistica, l'ulteriore sviluppo di EryDex, le richieste
di legge e le interazioni con le autorità di regolamentazione; il
potenziale terapeutico e commerciale; l'integrazione delle
attività, delle operazioni e dei dipendenti di EryDel in Quince; i
futuri progetti di sviluppo di Quince e le tempistiche relative; la
posizione di cassa dell'azienda e la strategia di cassa prevista;
l'attenzione, gli obiettivi, i programmi e le strategie
dell'azienda; e la capacità di eseguire qualsiasi transazione
strategica. Le dichiarazioni a carattere previsionale si basano
sulle aspettative attuali di Quince e sono soggette a incertezze,
rischi e presupposti intrinseci difficilmente prevedibili e che
potrebbero comportare una differenza sostanziale tra i risultati
effettivi e da quanto previsto dall'azienda. Alcune dichiarazioni a
carattere previsionale, inoltre, si basano su ipotesi relative a
eventi futuri che potrebbero dimostrarsi inaccurate. I fattori che
potrebbero comportare una differenza rispetto ai risultati
effettivi includono, ma non a titolo esaustivo, i rischi e le
incertezze descritte nella sezione "Risk Factors" (Fattori di
rischio) nella relazione trimestrale dell'azienda registrata sul
modulo 10-Q e depositata presso la Securities and Exchange
Commission (SEC) il 15 maggio 2023, e altri documenti sempre
depositati presso la SEC. Le dichiarazioni a carattere previsionale
contenute in questo comunicato stampa hanno valore a partire dalla
data presente e Quince non si assume alcun obbligo di aggiornare
tali informazioni, a eccezione di quanto imposto dalle leggi in
materia.
Il testo originale del presente annuncio, redatto nella lingua
di partenza, è la versione ufficiale che fa fede. Le traduzioni
sono offerte unicamente per comodità del lettore e devono rinviare
al testo in lingua originale, che è l'unico giuridicamente
valido.
Vedi la
versione originale su businesswire.com: https://www.businesswire.com/news/home/20230724010885/it/
Quince Therapeutics: Stacy Roughan Quince Therapeutics,
Inc. Vicepresidente per i Rapporti con gli investitori e le
comunicazioni aziendali ir@quincetx.com
Media: Dan Gagnier e Riyaz Lalani Gagnier Communications
quinceGFC@gagnierfc.com
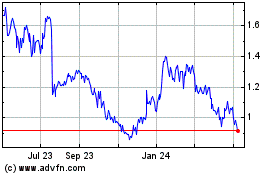
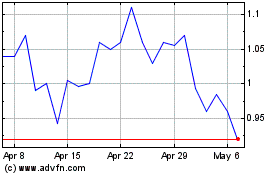
Quince Therapeutics (NASDAQ:QNCX)
Historical Stock Chart
From Jun 2024 to Jul 2024
Quince Therapeutics (NASDAQ:QNCX)
Historical Stock Chart
From Jul 2023 to Jul 2024