- Revenus totaux de 929 millions de dollars, soit une
augmentation de 56 % par rapport à l’année précédente ; réduction
de la perte d’exploitation PCGR et obtention d’un revenu
d’exploitation non-PCGR
- Renforcement du leadership en hématologie avec des revenus
globaux de BRUKINSA de 637 millions de dollars, soit une
augmentation de 107 % par rapport à la période de l’année
précédente ; avancement des programmes pivots pour l’inhibiteur de
BCL2 sonrotoclax et le dégradeur ciblant BTK BGB-16673
- Développement d’un pipeline innovant dans les tumeurs solides
comprenant plus de 15 molécules expérimentales, y compris des ADC,
des anticorps multispécifiques et des thérapies ciblées pour les
cancers du poumon, du sein et gastro-intestinaux
- Renforcement de la présence mondiale avec l’ouverture d’une
usine phare de fabrication de produits biologiques et d’un centre
de R&D clinique aux États-Unis, d’une superficie de 42
demi-hectares et d’une valeur de 800 millions de dollars, dans le
New Jersey, et proposition de redomiciliation des îles Caïmans vers
la Suisse, un écosystème biotechnologique innovant pour les leaders
et les institutions du secteur des sciences de la vie
BeiGene, Ltd. (NASDAQ : BGNE ; HKEX : 06160 ; SSE : 688235), une
société mondiale d’oncologie, a annoncé aujourd’hui ses résultats
du deuxième trimestre 2024 et des nouvelles qui renforcent la
société en vue d’une croissance mondiale future.
Ce communiqué de presse contient des éléments
multimédias. Voir le communiqué complet ici :
https://www.businesswire.com/news/home/20240807962849/fr/
(Graphic: Business Wire)
« Ce deuxième trimestre a été extraordinaire et a marqué un
point d’inflexion, BeiGene ayant atteint un résultat d’exploitation
non PCGR positif avec des revenus mondiaux en croissance rapide et
une discipline financière continue. Après avoir franchi cette
étape, nous allons continuer à développer nos capacités
stratégiques différenciées en tant que leader mondial de
l’innovation en oncologie », déclare John V. Oyler, cofondateur et
président-directeur général de BeiGene. « BRUKINSA s’impose comme
le leader de la classe BTKi aux États-Unis en termes de nouveaux
patients dans toutes les indications approuvées, démontrant la
solidité de ses données cliniques d’efficacité et de sécurité, et
est le seul BTKi à démontrer une efficacité supérieure à celle de
l’ibrutinib dans un essai en tête-à-tête. Forts de notre leadership
en hématologie, nous nous efforçons d’étendre nos activités à
d’autres types de cancer très répandus, en nous appuyant sur l’une
des plus grandes équipes de recherche en oncologie de l’industrie.
Grâce à notre croissance continue dans des centres
biopharmaceutiques établis tels que le New Jersey et la Suisse,
nous sommes mieux positionnés pour atteindre encore plus de
patients avec nos médicaments innovants. »
Principaux chiffres
financiers
(Montants en milliers de dollars américains)
Trois mois terminés le 30
juin
Six mois terminés le 30
juin
(en milliers, sauf
pourcentages)
2024
2023
% de changement
2024
2023
% de changement
Revenus nets des produits
$
921 146
$
553 745
66
%
$
1 668 064
$
964 036
73
%
Revenus nets des collaborations
$
8 020
$
41 516
(81
)%
$
12 754
$
79 026
(84
)%
Total des revenus
$
929 166
$
595 261
56
%
$
1 680 818
$
1 043 062
61
%
Perte d’exploitation PCGR
$
(107 161
)
$
(318 715
)
(66
)%
$
(368 509
)
$
(689 973
)
(47
)%
Résultat (perte) d’exploitation
ajusté*
$
48 464
$
(193 051
)
125
%
$
(98 877
)
$
(468 910
)
(79
)%
* Pour une explication de notre utilisation des mesures
financières non-PCGR, voir la section « Utilisation des mesures
financières non PCGR » plus loin dans ce communiqué de presse et
pour un rapprochement de chaque mesure financière non-PCGR avec les
mesures PCGR les plus comparables, voir le tableau à la fin de ce
communiqué de presse.
Principales nouvelles
commerciales
BRUKINSA® (zanubrutinib)
- Les ventes de BRUKINSA aux États-Unis ont totalisé 479 millions
de dollars au deuxième trimestre 2024, soit une croissance de 114 %
par rapport à la période de l’année précédente, plus de 60 % de la
croissance de la demande d’un trimestre à l’autre provenant de
l’utilisation élargie dans la LLC, BRUKINSA continuant à gagner des
parts dans le nombre de nouveaux patients atteints de LLC ; les
ventes de BRUKINSA en Europe ont totalisé 81 millions de dollars au
deuxième trimestre 2024, soit une croissance de 209 %, grâce à
l’augmentation de la part de marché sur tous les principaux
marchés, notamment l’Allemagne, l’Italie, l’Espagne, la France et
le Royaume-Uni ;
- Présentation des données de la branche D de l’essai de phase 3
SEQUOIA évaluant BRUKINSA en association avec le venetoclax chez
des patients naïfs de traitement (TN) atteints de LLC à haut risque
et/ou de lymphome lymphocytaire de petite taille (SLL) avec
del(17p) et/ou mutation TP53 lors d’une présentation orale au
congrès hybride 2024 de l’Association européenne d’hématologie
(EHA) ; les données préliminaires ont démontré un taux de réponse
globale de 100 % chez 65 patients évaluables pour la réponse et un
taux de réponse complète (RC) plus RC avec récupération
hématopoïétique incomplète (RCi) de 48 % ; et
- Présentation de nouvelles analyses mettant en évidence
l’amélioration de la survie sans progression et des taux de
réponse, ainsi qu’une faible utilisation de médicaments
antihypertenseurs chez les patients traités par BRUKINSA par
rapport à d’autres inhibiteurs de la tyrosine kinase (BTKi) de
Bruton utilisés pour traiter la LLC/SLL, notamment l’acalabrutinib
et l’ibrutinib, lors de l’assemblée annuelle de l’American Society
of Clinical Oncology (ASCO) et de l’EHA.
TEVIMBRA® (tislelizumab)
- Les ventes de tislelizumab ont totalisé 158 millions de dollars
au deuxième trimestre 2024, soit une croissance de 6 % par rapport
à la période de l’année précédente ;
- Présentation de nouvelles données de l’étude de phase 3
RATIONALE-306 évaluant TEVIMBRA en association avec une
chimiothérapie chez des patients atteints d’un carcinome
épidermoïde de l’œsophage (ESCC) avancé ou métastatique à l’ASCO ;
et
- La Food and Drug Administration (FDA) des États-Unis a reporté
l’approbation du tislelizumab dans le traitement en première
intention de l’ESCC non résécable, récurrent, localement avancé ou
métastatique, avec une date d’action PDUFA cible de juillet 2024,
en raison d’un retard dans la programmation des inspections des
sites cliniques.
Principales caractéristiques du
pipeline
Hématologie Sonrotoclax (inhibiteur de BCL2)
- Plus de 1 000 patients ont été recrutés à ce jour dans
l’ensemble du programme ;
- Achèvement du recrutement dans l’essai mondial de phase 2 dans
le lymphome à cellules du manteau R/R (MCL) et poursuite du
recrutement dans l’essai mondial de phase 2 dans la
macroglobulinémie de Waldenstr�m (WM) et dans l’essai de phase 2 en
Chine uniquement dans la LLC R/R, tous avec une intention
d’enregistrement, ainsi que poursuite du recrutement dans l’essai
mondial de phase 3 CELESTIAL en association avec BRUKINSA dans la
LLC TN ;
- Lors de l’EHA 2024, présentation de données mettant en évidence
des réponses profondes et durables avec un profil de sécurité
tolérable dans les études de phase 1 en combinaison avec BRUKINSA
dans la LLC/SLL R/R et la MCL R/R, ainsi que des résultats d’essais
de phase 1 supplémentaires démontrant des taux de réponse
encourageants, des réponses durables et des profils de sécurité
gérables en monothérapie dans la MW R/R, en combinaison avec
l’azacitidine dans la leucémie myéloïde aiguë TN et R/R, et en
combinaison avec la dexaméthasone dans le myélome multiple R/R
hébergeant une translocation (11;14) ;
- Obtention d’une désignation accélérée de la FDA pour R/R WM ;
et
- Les premiers sujets recrutés dans les programmes de phase 3
pour la LLC R/R et la MCL R/R devraient être recrutés au quatrième
trimestre 2024 ou au premier trimestre 2025.
BGB-16673 (BTK CDAC)
- Plus de 300 patients recrutés à ce jour dans l’ensemble du
programme ; poursuite du recrutement de cohortes potentiellement
enregistrables permettant l’expansion des cohortes dans la MCL R/R
et la CLL R/R ; et
- Lors de l’EHA 2024, présentation de données mettant en évidence
une efficacité et une sécurité préliminaires prometteuses chez des
patients atteints de LLC/SLL R/R ; anticipation du recrutement du
premier sujet dans le programme de phase 3 au quatrième trimestre
2024 ou au premier trimestre 2025.
Tumeurs solides Cancer du poumon
- Plusieurs cohortes randomisées de combinaison de tislelizumab
pour le cancer du poumon avec BGB-A445 (anti-OX40), LBL-007
(anti-LAG3) et BGB-15025 (inhibiteur de HPK1) dont les résultats
sont attendus en 2024 ;
- BGB-C354 (B7H3 ADC) : début de dose croissante pour le premier
ADC développé en interne par la société ;
- BGB-R046 (promédicament de l’IL-15) : début de dose croissante
; il s’agit d’un promédicament de cytokine, qui tire parti de la
libération dépendante des protéases de l’IL-15 actif dans le
microenvironnement tumoral et déclenche une activité antitumorale
en favorisant l’expansion des cellules T et des cellules tueuses
naturelles (NK) ; et
- Pan-KRAS, inhibiteurs de PRMT5 MTA-coopératifs et dégradeur de
protéines ciblé EGFR CDAC en voie d’entrée en clinique au second
semestre 2024.
Cancers du sein et gynécologiques
- BGB-43395 (inhibiteur de CDK4) : poursuite de la dose
croissante en monothérapie et en association avec le fulvestrant et
le létrozole dans la gamme de doses efficaces anticipées, sans
observation de toxicités limitant la dose ; plus de 60 patientes
recrutées à ce jour dans l’ensemble du programme ; possibilité de
partager la première lecture des données de la phase 1 au quatrième
trimestre 2024 ; et
- BG-68501 (inhibiteur de CDK2) et BG-C9074 (ADC B7H4) :
poursuite de la dose croissante en monothérapie, avec une
pharmacocinétique conforme aux attentes et aucune toxicité limitant
la dose n’a été observée.
Cancers gastro-intestinaux
- Cohortes de combinaison du tislelizumab avec LBL-007
(anti-LAG3) dans l’ESCC, relevé en 2024 ;
- BLA acceptée par le NMPA pour le zanidatamab dans le traitement
en deuxième ligne du cancer des voies biliaires ; et
- CEA ADC, FGFR2b ADC et anticorps bispécifique GPC3x4-1BB en
voie d’entrer en clinique au second semestre 2024.
Immunologie et inflammation
- Début du développement clinique du BGB-43035 (CDAC IRAK4) qui a
le potentiel d’induire une dégradation plus profonde et plus rapide
d’IRAK4 avec une inhibition plus forte des cytokines que les
concurrents ; il s’agit du deuxième dégradeur ciblé issu de la
plateforme CDAC propriétaire de l’entreprise.
Actualités de
l’entreprise
- Ouverture d’une usine de fabrication de produits biologiques et
d’un centre de R&D clinique au Princeton West Innovation Campus
à Hopewell, N.J. ; l’usine comprend 400 000 pieds carrés d’espace
de fabrication dédié ; et
- Annonce de l’intention de changer la juridiction
d’incorporation des îles Caïmans à Bâle, en Suisse, permettant à la
société d’approfondir ses racines dans un centre biopharmaceutique
mondial tandis qu’elle continue à exécuter sa stratégie de
croissance mondiale pour atteindre plus de patients dans le monde
avec ses médicaments innovants ; cette redomiciliation est sujette
à l’approbation des actionnaires.
Chiffres financiers du deuxième
trimestre 2024
Les recettes pour les trois mois clos le 30 juin 2024 se
sont élevées à 929 millions de dollars, contre 595 millions de
dollars pour la même période de 2023, principalement en raison de
la croissance des ventes de produits BRUKINSA aux États-Unis et en
Europe, respectivement de 114 % et 209 %.
Les recettes de produits pour le trimestre clos le 30
juin 2024 se sont élevées à 921 millions de dollars, contre 554
millions de dollars pour la même période de 2023, soit une
augmentation de 66 %. L’augmentation des revenus des produits est
principalement attribuable à l’augmentation des ventes de BRUKINSA.
Pour le trimestre clos le 30 juin 2024, les États-Unis ont été le
plus grand marché de la société, avec des recettes de produits de
479 millions de dollars, contre 224 millions de dollars pour la
période de l’année précédente. Outre la croissance des revenus de
BRUKINSA, les revenus des produits ont été positivement influencés
par les ventes de produits sous licence d’Amgen en Chine et de
tislelizumab.
La marge brute, exprimée en pourcentage du chiffre
d’affaires global des produits pour le deuxième trimestre 2024,
était de 85 %, contre 83 % pour la période de l’année précédente.
Le pourcentage de marge brute a augmenté principalement en raison
d’une composition mondiale des ventes proportionnellement plus
élevée de BRUKINSA par rapport aux autres produits du
portefeuille.
Frais d’exploitation
Le tableau suivant résume les dépenses d’exploitation pour le
deuxième trimestre 2024 et 2023, respectivement :
PCGR
Non-PCGR
(en milliers, sauf
pourcentages)
2e trimestre 2024
2e trimestre 2023
% de changement
2e trimestre 2024
2e trimestre 2023
%
Recherche et développement
$
454 466
$
422 764
7
%
$
382 509
$
363 735
5
%
Frais de vente, généraux et
administratifs
$
443 729
$
395 034
12
%
$
363 922
$
331 607
10
%
Amortissement
$
—
$
188
(100
)%
$
—
$
—
NM
Dépenses d’exploitation totales
$
898 195
$
817 986
10
%
$
746 431
$
695 342
7
%
Le tableau suivant résume les dépenses d’exploitation pour les
premiers semestres 2024 et 2023, respectivement :
PCGR
Non-PCGR
(en milliers, sauf
pourcentages)
2e trimestre en cumul annuel
2024
2e trimestre en cumul annuel
2023
% de changement
2e trimestre en cumul annuel
2024
2e trimestre en cumul annuel
2023
% de changement
Recherche et développement
$
915 104
$
831 348
10
%
$
787 949
$
725 431
9
%
Frais de vente, généraux et
administratifs
$
871 156
$
723 533
20
%
$
736 068
$
614 761
20
%
Amortissement
$
—
$
375
(100
)%
$
—
$
—
NM
Dépenses d’exploitation totales
$
1 786 260
$
1 555 256
15
%
$
1 524 017
$
1 340 192
14
%
Les dépenses de recherche et développement (R&D) ont
augmenté au deuxième trimestre 2024 par rapport à la période de
l’année précédente, à la fois sur une base PCGR et ajustée,
principalement en raison de l’avancement des programmes
précliniques vers la clinique et des programmes cliniques précoces
vers un stade avancé. Les paiements initiaux et les paiements
d’étape liés à la R&D en cours pour les actifs sous licence ont
totalisé 12 millions de dollars au deuxième trimestre 2024, contre
zéro pour la période de l’année précédente.
Les frais de vente, généraux et administratifs (SG&A)
ont augmenté au deuxième trimestre 2024 par rapport à la période de
l’année précédente, à la fois sur une base PCGR et ajustée, en
raison de l’investissement continu dans le lancement commercial
mondial de BRUKINSA, principalement aux États-Unis et en Europe.
Les frais de vente et d’administration, exprimés en pourcentage des
ventes de produits, se sont élevés à 48 % pour le deuxième
trimestre 2024, contre 71 % pour la période de l’année
précédente.
Bénéfice (perte) d’exploitation au deuxième trimestre
2024, la perte d’exploitation a diminué de 66 % sur une base PCGR.
Sur une base ajustée, nous avons réalisé un bénéfice d’exploitation
de 48 millions de dollars. La diminution de la perte d’exploitation
selon les PCGR et l’atteinte de la rentabilité sur une base ajustée
est un objectif stratégique clé et le résultat d’efforts
considérables pour stimuler la croissance tout en maintenant une
discipline d’investissement.
La perte nette PCGR s’est améliorée pour le trimestre
clos le 30 juin 2024 par rapport à la période de l’année
précédente, car la croissance des revenus de nos produits et la
gestion des dépenses entraînent une augmentation du levier
d’exploitation.
Pour le trimestre clos le 30 juin 2024, la perte nette par
action était de (0,09) $ et (1,15) $ par American Depositary Share
(ADS), contre (0,28) $ par action et (3,64) $ par ADS pour la
période de l’année précédente.
Les liquidités utilisées dans les opérations pour le
trimestre clos le 30 juin 2024 ont totalisé 96 millions de dollars,
contre 294 millions de dollars pour la période de l’année
précédente, grâce à l’amélioration de l’effet de levier
opérationnel.
Pour plus de détails sur les états financiers du deuxième
trimestre 2024 de BeiGene, veuillez consulter le rapport
trimestriel de BeiGene sur le formulaire 10-Q pour le deuxième
trimestre 2024 déposé auprès de la Securities and Exchange
Commission des États-Unis.
À propos de BeiGene
BeiGene est une société internationale d’oncologie qui découvre
et développe des traitements innovants plus abordables et
accessibles aux patients atteints de cancer dans le monde entier.
Avec un large portefeuille, nous accélérons le développement de
notre pipeline diversifié de nouvelles thérapies grâce à nos
capacités internes et à nos collaborations. Nous nous engageons à
améliorer radicalement l’accès aux médicaments pour un plus grand
nombre de patients qui en ont besoin. Notre équipe mondiale en
pleine croissance compte plus de 10 000 collègues répartis sur les
cinq continents. Pour en savoir plus sur BeiGene, rendez-vous sur
www.beigene.com et suivez-nous sur LinkedIn, X (anciennement
Twitter) et Facebook.
Déclarations prospectives
Ce communiqué de presse contient des déclarations prospectives
au sens du Private Securities Litigation Reform Act de 1995 et
d’autres lois fédérales sur les valeurs mobilières, y compris des
déclarations concernant le potentiel de BeiGene à émerger davantage
en tant qu’innovateur mondial de premier plan en oncologie ; la
capacité de BeiGene à s’étendre à d’autres types de cancer à forte
prévalence ; les données et activités cliniques préliminaires de
BeiGene, ainsi que les résultats attendus ; l’approbation par les
actionnaires du changement de juridiction d’incorporation de
BeiGene et, le cas échéant, le fait que ce changement permettra à
BeiGene de poursuivre l’exécution de sa stratégie de croissance
mondiale ; et les plans, engagements, aspirations et objectifs de
BeiGene sous la rubrique « À propos de BeiGene ». Les résultats
réels peuvent différer matériellement de ceux indiqués dans les
déclarations prospectives en raison de divers facteurs importants,
y compris la capacité de BeiGene à démontrer l’efficacité et la
sécurité de ses médicaments candidats ; les résultats cliniques de
ses médicaments candidats, qui peuvent ne pas soutenir la poursuite
du développement ou l’autorisation de mise sur le marché ; les
actions des organismes de réglementation, qui peuvent affecter le
lancement, le calendrier et le progrès des essais cliniques et
l’autorisation de mise sur le marché ; la capacité de BeiGene à
atteindre le succès commercial pour ses médicaments commercialisés
et ses médicaments candidats, s’ils sont approuvés ; la capacité de
BeiGene à obtenir et à maintenir la protection de la propriété
intellectuelle pour ses médicaments et sa technologie ; la
dépendance de BeiGene à l’égard de tiers pour le développement, la
fabrication et la commercialisation de médicaments et d’autres
services ; l’expérience limitée de BeiGene en matière d’obtention
d’autorisations réglementaires et de commercialisation de produits
pharmaceutiques ; et la capacité de BeiGene à obtenir des fonds
supplémentaires pour ses opérations et à achever le développement
de ses médicaments candidats et à atteindre et maintenir la
rentabilité ; et les risques plus amplement décrits dans la section
intitulée « Facteurs de risque » du dernier rapport trimestriel de
BeiGene sur formulaire 10-Q, ainsi que les discussions sur les
risques potentiels, les incertitudes et d’autres facteurs
importants dans les documents déposés ultérieurement par BeiGene
auprès de la U.S. Securities and Exchange Commission. Toutes les
informations contenues dans le présent communiqué de presse sont à
jour et BeiGene ne s’engage pas à mettre à jour ces informations,
sauf si la loi l’exige.
États consolidés condensés des opérations
(PCGR États-Unis)
(Montants en milliers de dollars américains,
sauf pour les actions, American Depositary Shares (ADS), données
par action et par ADS)
Trois mois terminés
30 juin
Six mois terminés
30 juin
2024
2023
2024
2023
(Non audité)
(Non audité)
Chiffre d’affaires
Revenus des produits, nets
$
921 146
$
553 745
$
1 668 064
$
964 036
Revenus de collaboration
8 020
41 516
12 754
79 026
Total des revenus
929 166
595 261
1 680 818
1 043 062
Coût des ventes - produits
138 132
95 990
263 067
177 779
Bénéfice brut
791 034
499 271
1 417 751
865 283
Frais d’exploitation :
Recherche et développement
454 466
422 764
915 104
831 348
Frais de vente, généraux et
administratifs
443 729
395 034
871 156
723 533
Amortissement des actifs incorporels
—
188
—
375
Dépenses d’exploitation totales
898 195
817 986
1 786 260
1 555 256
Perte d’exploitation
(107 161
)
(318 715
)
(368 509
)
(689 973
)
Intérêts créditeurs, nets
13 225
15 070
29 385
31 086
Autres dépenses, nettes
(11 984
)
(63 818
)
(10 222
)
(45 515
)
Perte avant impôts sur le revenu
(105 920
)
(367 463
)
(349 346
)
(704 402
)
Charge d’impôt sur le revenu
14 485
13 674
22 209
25 166
Perte nette
(120 405
)
(381 137
)
(371 555
)
(729 568
)
Perte nette par action, de base et
diluée
$
(0,09
)
$
(0,28
)
$
(0,27
)
$
(0,54
)
Nombre moyen pondéré d’actions en
circulation, de base et dilué
1 361 082 567
1 360 224 377
1 358 315 145
1 357 211 308
Perte nette par ADS, de base et diluée
$
(1,15
)
$
(3,64
)
$
(3,56
)
$
(6,99
)
Moyenne pondérée des ADS en circulation,
de base et diluée
104 698 659
104 632 644
104 485 780
104 400 870
Données du bilan consolidé condensé (PCGR
États-Unis)
(Montants en milliers de dollars
américains)
Au
30 juin
31 décembre
2024
2023
(non audité)
(audité)
Actifs :
Trésorerie, équivalents de trésorerie et
liquidités soumises à restrictions
$
2 617 931
$
3 185 984
Créances, nettes
529 449
358 027
Inventaires
443 260
416 122
Immobilisations corporelles, nettes
1 516 491
1 324 154
Total des actifs
5 712 179
5 805 275
Passif et capitaux propres :
Comptes à payer
333 022
315 111
Charges à payer et autres dettes
646 538
693 731
Passif lié au partage des coûts de
R&D
203 627
238 666
Dettes
1 036 928
885 984
Total des passifs
2 345 924
2 267 948
Total des capitaux propres
$
3 366 255
$
3 537 327
Note concernant l’utilisation de mesures financières
non-PCGR
BeiGene fournit certaines mesures financières non-PCGR, y
compris les frais d’exploitation ajustés et la perte d’exploitation
ajustée, ainsi que certains autres postes du compte de résultat
non-PCGR, chacun d’entre eux comprenant des ajustements aux
chiffres des PCGR. Ces mesures financières non-PCGR sont destinées
à fournir des informations supplémentaires sur la performance
opérationnelle de BeiGene. Les ajustements aux chiffres PCGR de
BeiGene excluent, le cas échéant, les éléments non monétaires tels
que les rémunérations basées sur des actions, les dépréciations et
les amortissements. Certains autres éléments spéciaux ou événements
importants peuvent également être inclus dans les ajustements
non-PCGR périodiquement lorsque leur ampleur est significative dans
les périodes concernées. BeiGene maintient une politique non-PCGR
établie qui guide la détermination des coûts qui seront exclus dans
les mesures financières non-PCGR et les protocoles, contrôles et
approbations liés à l’utilisation de ces mesures. BeiGene estime
que ces mesures financières non-PCGR, lorsqu’elles sont considérées
conjointement avec les chiffres PCGR, peuvent améliorer la
compréhension globale de la performance opérationnelle de BeiGene.
Les mesures financières non-PCGR sont incluses dans le but de
fournir aux investisseurs une compréhension plus complète des
résultats financiers historiques et attendus de la société et des
tendances, et de faciliter les comparaisons entre les périodes et
par rapport aux informations projetées. En outre, ces mesures
financières non-PCGR font partie des indicateurs que la direction
de BeiGene utilise à des fins de planification et de prévision et
pour mesurer la performance de la société. Ces mesures financières
non-PCGR doivent être considérées comme un complément et non comme
un substitut ou une supériorité aux mesures financières calculées
conformément aux PCGR. Les mesures financières non-PCGR utilisées
par l’entreprise peuvent être calculées différemment des mesures
financières non-PCGR utilisées par d’autres entreprises et, par
conséquent, ne pas être comparables à ces dernières.
RAPPROCHEMENT D’UNE SÉLECTION DE MESURES
PCGR ET NON-PCGR
(en milliers, sauf les montants par
action)
(non audité)
Trois mois terminés
Six mois terminés
30 juin
30 juin
2024
2023
2024
2023
(en milliers)
(en milliers)
Rapprochement entre le coût des ventes
PCGR et le coût des ventes ajusté - produits :
Coût des ventes PCGR - produits
$
138 132
$
95 990
$
263 067
$
177 779
Moins : Dépréciation
2 684
2 180
5 029
4 360
Moins : Amortissement des immobilisations
incorporelles
1 177
840
2 360
1 639
Coût des ventes ajusté - produits
$
134 271
$
92 970
$
255 678
$
171 780
Rapprochement entre les PCGR et la
recherche et développement ajustée :
Recherche et développement PCGR
$
454 466
$
422 764
$
915 104
$
831 348
Moins : Coûts liés aux rémunérations
fondées sur des actions
55 406
45 948
93 451
79 976
Moins : Dépréciation
16 551
13 081
33 704
25 941
Recherche et développement ajustée
$
382 509
$
363 735
$
787 949
$
725 431
Rapprochement entre les PCGR et les
frais de vente, généraux et administratifs ajustés :
Frais de vente et d’administration
PCGR
$
443 729
$
395 034
$
871 156
$
723 533
Moins : Coûts liés aux rémunérations
fondées sur des actions
75 288
57 381
125 957
98 741
Moins : Dépréciation
4 519
6 046
9 131
10 031
Frais de vente, généraux et administratifs
ajustés
$
363 922
$
331 607
$
736 068
$
614 761
Rapprochement des frais d’exploitation
ajustés et des frais d’exploitation PCGR
Charges d’exploitation PCGR
$
898 195
$
817 986
$
1 786 260
$
1 555 256
Moins : Coûts liés aux rémunérations
fondées sur des actions
130 694
103 329
219 408
178 717
Moins : Dépréciation
21 070
19 127
42 835
35 972
Moins : Amortissement des immobilisations
incorporelles
—
188
—
375
Charges d’exploitation ajustées
$
746 431
$
695 342
$
1 524 017
$
1 340 192
Rapprochement du bénéfice (perte)
d’exploitation ajusté(e) et du bénéfice (perte) d’exploitation
conforme aux PCGR :
Perte d’exploitation PCGR
$
(107 161
)
$
(318 715
)
$
(368 509
)
$
(689 973
)
Plus : Coûts liés aux rémunérations
fondées sur des actions
130 694
103 329
219 408
178 717
Plus : Dépréciation
23 754
21 307
47 864
40 332
Plus : Amortissement des immobilisations
incorporelles
1 177
1 028
2 360
2 014
Résultat (perte) d’exploitation ajusté
$
48 464
$
(193 051
)
$
(98 877
)
$
(468 910
)
Le texte du communiqué issu d’une traduction ne doit d’aucune
manière être considéré comme officiel. La seule version du
communiqué qui fasse foi est celle du communiqué dans sa langue
d’origine. La traduction devra toujours être confrontée au texte
source, qui fera jurisprudence.
Consultez la
version source sur businesswire.com : https://www.businesswire.com/news/home/20240807962849/fr/
Contact investisseurs Liza Heapes +1 857-302-5663
ir@beigene.com
Contact médias Kyle Blankenship +1 667-351-5176
media@beigene.com
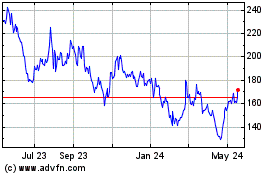
BeiGene (NASDAQ:BGNE)
Historical Stock Chart
From Sep 2024 to Oct 2024
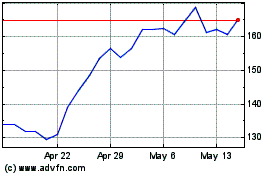
BeiGene (NASDAQ:BGNE)
Historical Stock Chart
From Oct 2023 to Oct 2024